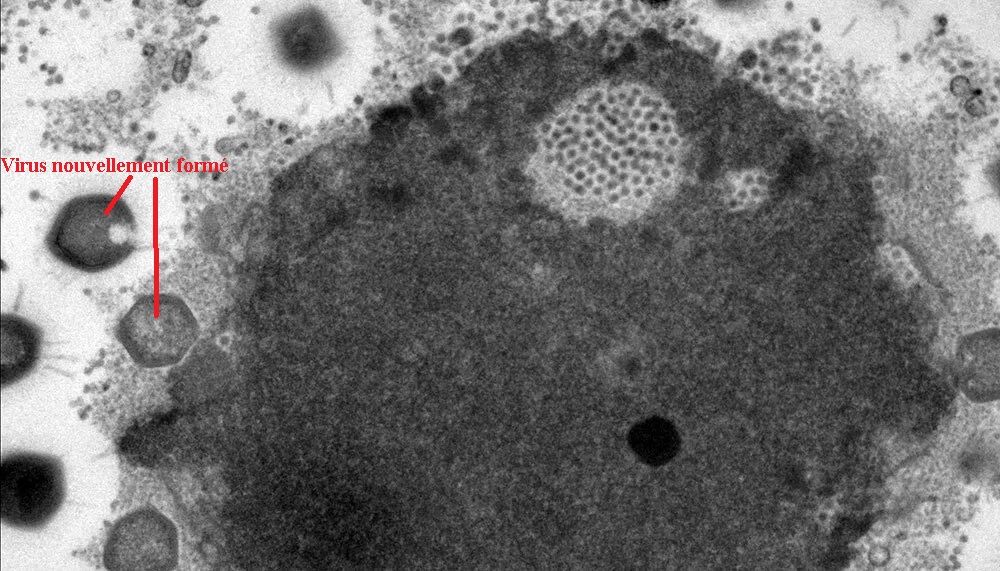
Notions de virologie:
Les virus :
Je vais développer trois thèmes importants qui seront la définition, la structure et la classification des virus.
Avec les éléments que vous avez acquis en lisant les précédents chapitres, il sera aisé pour vous d’appréhender ce qui suit.
La notion de maladie virale remonte à la fin du 19e siècle, période à laquelle Pasteur, Ivanowski, Toeffler et Frosch démontrèrent respectivement pour une maladie pouvant atteindre l'homme avec la rage, les végétaux avec la mosaïque du tabac et les animaux comme la fièvre aphteuse, la résistance d'un agent ultrafiltrable pouvant passer à travers les pores de filtre en porcelaine connue pour retenir les bactéries. Cet agent pathogène invisible au microscope optique est responsable d'infections transmissibles en série.
Longtemps défini par leur taille, les virus constituent un groupe d'être biologique distinct des êtres vivants à structure cellulaire classique et comportant un très grand nombre d'espèces différentes, infectant pratiquement tous les genres d'animaux (y compris les arthropodes), les végétaux (même les algues et les champignons), les protistes et en particulier les bactéries (bactériophages).
On dénombre à peu près 1400 espèces de virus pathogènes pour l'homme d'après l'institut Pasteur.
Le domaine pathologique des virus est étendu et varié. Certaines affections virales bénignes sont caractéristiques de leur grande fréquence (coryza saisonnier, verrues et fièvre éruptive de l'enfance,...). D'autres plus rares présentent une gravité certaine (poliomyélite, fièvre jaune par exemple). Certaines sont redoutables quand elles atteignent des terrains particuliers comme la femme enceinte avec la rubéole, la maladie des inclusions cytoplasmiques ou des sujets au système immunitaire déficient comme avec l’herpès, la varicelle zona et le HIV. Certains virus jouent un rôle dans le développement de certaines tumeurs malignes chez l'homme (virus d'Epstein Barr et lymphome malin, virus de l'herpès simplex type 2, carcinome du col utérin...).
A/ Caractère de définition :
1/ Chaque particule ne contient qu'un type d'acide nucléique soit de l'ARN soit de l'ADN. Cet acide nucléique constitue le génome viral. Ce caractère oppose les virus aux êtres vivants à structure cellulaire chez lesquels il y a à la fois l'ADN qui conserve l'information génétique et l'ARN qui permet l'expression génétique.
2/Les virus se reproduisent uniquement à partir de matériel génétique par réplication. Il ne se divise pas par scissiparité comme les bactéries et ne subissent pas de phénomènes analogues à la mitose des cellules eucaryotes.
3/ les virus sont doués d'un parasitisme intracellulaire absolu. Leur structure simple les conduit à ne pouvoir se reproduire qu'au sein d'une cellule. En effet, le virus, limité par une information génétique protégée par des structures périphériques, ne possède aucun système enzymatique ou énergétique lui permettant d'assurer sa propre réplication. Il doit donc détourner pour sa propre biosynthèse l'ensemble des coordonnées des macromolécules de la cellule qu’il parasite (ribosome, ARN, activités enzymatiques diverses, système de régulation,...). Du coup, les virus sont incapables de se reproduire sur des milieux inertes de type bactériologique, leur isolement passe forcément par l'inoculation à un système biologique vivant dit permissif, capable d'assurer leur réplication. Par conséquent, l'infection virale représente une forme particulièrement élaborée de parasitisme où une information génétique isolée détourne à son profit certains éléments du métabolisme de la cellule infectée et assure très efficacement sa pérennisation. Par ailleurs, les trois tests des contacts entre le virus et la cellule hôte au cours de la multiplication expliquent la difficulté de mise au point d'une chimiothérapie antivirale spécifique à la fois efficace, non dangereuse et raisonnablement utilisable en thérapeutique humaine. Enfin ce mode de reproduction particulier explique l'insensibilité des virus à la majorité des antibiotiques bactériens qui ne ciblent pas les mêmes sites bactériologiques.
4/ Les virus présentent une structure particulière qui les oppose aux êtres vivants à structure cellulaire procaryote ou eucaryote. On nomme virion la particule virale mature, infectieuse et extracellulaire. C'est à partir de cette forme que se décime le virus en assurant le transfert de l'infection aux cellules et à d'autres organismes. Le virus est un objet biologique original, entièrement différent des micro-organismes classiques et en particulier des bactéries et des parasites. Cette structure et ce mode de reproduction particulier conditionne leur propriété biologique et leur pouvoir pathogène.
A la vue de tout cela on peut dire que les virus sont capables de se multiplier à grande vitesse mais sont-ils des êtres vivants ? Un organisme vivant naît, se nourrit, grandit, se reproduit et meurt. Le virus est dépourvu de métabolisme et semble plus près de la matière inerte, mais le fait qu’il se reproduise les rattache au vivant.

B/ Structures:
1/ Structure générale d'une particules virale :
Toutes les particule virale est composée de deux éléments constants :
- le génome composé d'acide nucléique et la capsule, coque de nature protéique entourant le génome. L'ensemble constitue une unité fonctionnelle nucléocapside. Pour certains virus seulement, c'est nucléocapside et elle-même entourée d'une structure appelée enveloppe ou péplos.
2/ L'acide nucléique virale:
Le génome viral contient l'intégralité de l'information génétique de la particule. Il est constitué soit d'ADN soit d'ARN mais dans tous les cas. La capacité de codage de l'acide nucléique virale est faible en général, de quelques unités à quelques centaines de gènes au maximum, mais certains virus géants comme le mimivirus ou le mégavirus peuvent coder plus 1200 gènes.
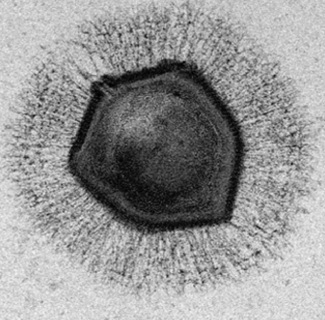
source:https://museum.toulouse-metropole.fr/des-virus-xxl-qui-bouleversent-les-dogmes-de-la-virologie/
Mimivirus fait 0,7 µm, soit trois fois plus que la longueur connue des virus à l'époque de sa découverte, qui était de 0,2 µm.
De nombreux cousins aux mimivirus ont ensuite été découverts, comme les pandoravirus, les pithovirus et autres mollivirus
a/ génome à ADN :
Ils sont très variés et leur poids moléculaire peut aller comme pour les papovaviridae de 3.106 daltons à environ 1000.106 daltons comme pour le mimivirus. Leur structure est souvent bicaténaire mais il existe des virus à ADN monocaténaire parvoviridae. Dans la majorité des cas, l'ADN est linéaire mais il existe quelques exceptions comme pour le Papovaviridae et le virus de l'hépatite B, les Redondoviridae ,... qui possèdent un ADN circulaire.
b/Génome ARN
Le poids moléculaire des ARN viraux va de 2,5.106daltons comme pour les picornaviridae et jusqu’à 15.106 daltons par exemple les Reoviridae. Les ARN sont généralement monocaténaires et linéaires sauf dans le cas des Réoviridae où le génome est bicaténaire. Le génome des virus grippaux et des Réovirida est constitué de plusieurs fragments reliés par des liaisons non covalentes. Cette disposition favorise les recombinaisons génétiques entre virus grippaux et permet l'expression d'une grande variété génétique et donc antigénique.
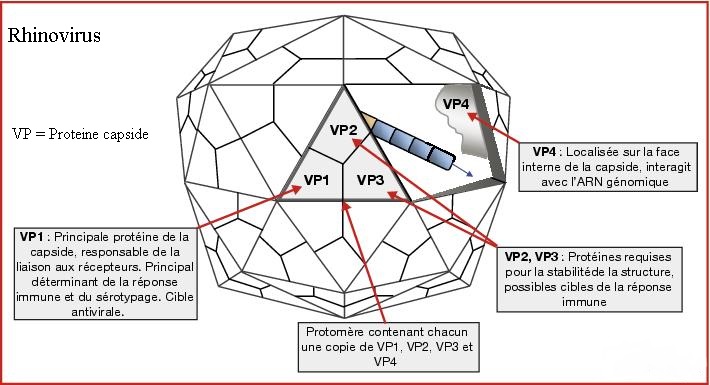
3/La capside :
Elle a essentiellement un rôle de protection du génome viral. C'est une structure polymérisée à base de sous-unité protéique. La quantité d'acide nucléique d'un virus étant faible, elle ne peut coder que pour un petit nombre de polypeptides différents. Ainsi les capsides sont constituées par la répétition d'une seule ou de quelques sous unités protéiques. selon les rapports que ces sous unités protéique contractent entre elles et avec l'acide nucléique, on définit deux types de nucléocapside virale :
a/ dans les nucléocapside à symétrie hélicoïdales, d'aspect tubulaire, les sous-unités protéiques s'assemble en manchon autour de l'acide nucléique et l'ensemble constitue un tubule plus ou moins rigide.
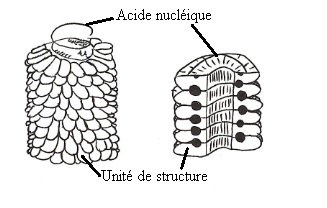
De nombreux virus animaux, et en particulier les Orthomyxoviridae et les Paramyxoviridae et ont une nucléocapside à symétrie hélicoïdale du même type.Cependant, à la différence de celle des virus des plantes, elle est flexible, enrouler sur elle-même et toujours incluse dans une enveloppe, ce qui lui donne au microscope électronique une morphologie symétrique.
b/ Dans les nucléocapsides icosaédrique à symétrie cubique, les unités de structure protéique se groupent en unités morphologiques appelées capsomères. Le groupement peut se faire par 5 aboutissants à un pentamère ou Peton ou encore par 6 donnant naissance à un hexamère ou Hexon. Ces capsomères sont eux-mêmes regroupés, pour constituer une figure géométrique : L’Icosaèdre.
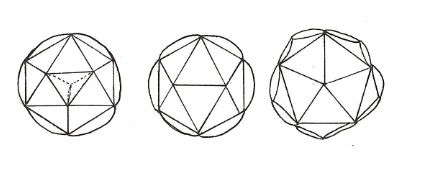
Enfin , chez certains virus l’acide nucléique est relié à des protéines internes, généralement basiques et peu actives antigénétiquement. L'ensemble protéine interne acide nucléique constitue le nucléoïde du virion ou Core.
4/ l'enveloppe virale :
de composition lipidoglucido protéique, l'enveloppe virale est un élément propre à certains virus seulement : les virus enveloppés et se dépourvu d'enveloppe.
L'enveloppe virale provient de des systèmes membranaires de la cellule hôte par bourgeonnement. 3 origines sont possibles :
-la membrane nucléaire ( herpesviridae).
- intra cytoplasmiques comme le réticulum endoplasmique ou l'appareil de Golgi (herpesviridae, Togaviridae).
-La membrane cytoplasmique (ortho et paramyxoviridae).
L'enveloppe virale située à la périphérie du virion porte des protéines ou glycoprotéines codées par le génome viral appelé péplomeres qui se fixe dans les membranes cellulaires au moment de la biosynthèse du virus. On trouve souvent à ce niveau des protéines à activité biologiques particulière (hémagglutinine, neuraminidases, facteurs de fusion cellulaire. Souvent ces formations sont visibles au microscope électronique sous forme de spicules. Enfin, il faut noter que l'enveloppe, très sensible aux divers agents physico-chimiques et en particulier au solvant des lipides (détergents, éthers, sels biliaires) et à la chaleur ne constitue pas un élément de protection supplémentaire de la particule. Au contraire, c'est un élément de fragilité rendant les virus peu résistants dans les milieux extérieurs. Du coup, cela a des conséquences en épidémiologie (faible persistance dans le milieu extérieur et dans les selles, transmission par contact immédiat et rapproché) et pour le diagnostic (faible probabilité de trouver le virus dans certains niveaux défavorables comme les matières fécales et nécessité d'un transport rapide du produit pathologique au laboratoire en vue de l'isolement du virus).
C/Classification des virus :
a/
Depuis 1960 un système de classification dit LHT se base sur 4 caractères objectifs de classification :
-la nature de l'acide nucléique permettant de distinguer les virus à ADN D des virus à ARN R.
-la symétrie de la nucléocapside, hélicoïdal H ou cubique C.
-la présence d'une enveloppe, les virus qui en possèdent étant dits E et les autres nus N.
-le nombre de capsomères dans le cas des virus icosaédrique ou le diamètre de la nucléocapside si elle est hélicoïdale.
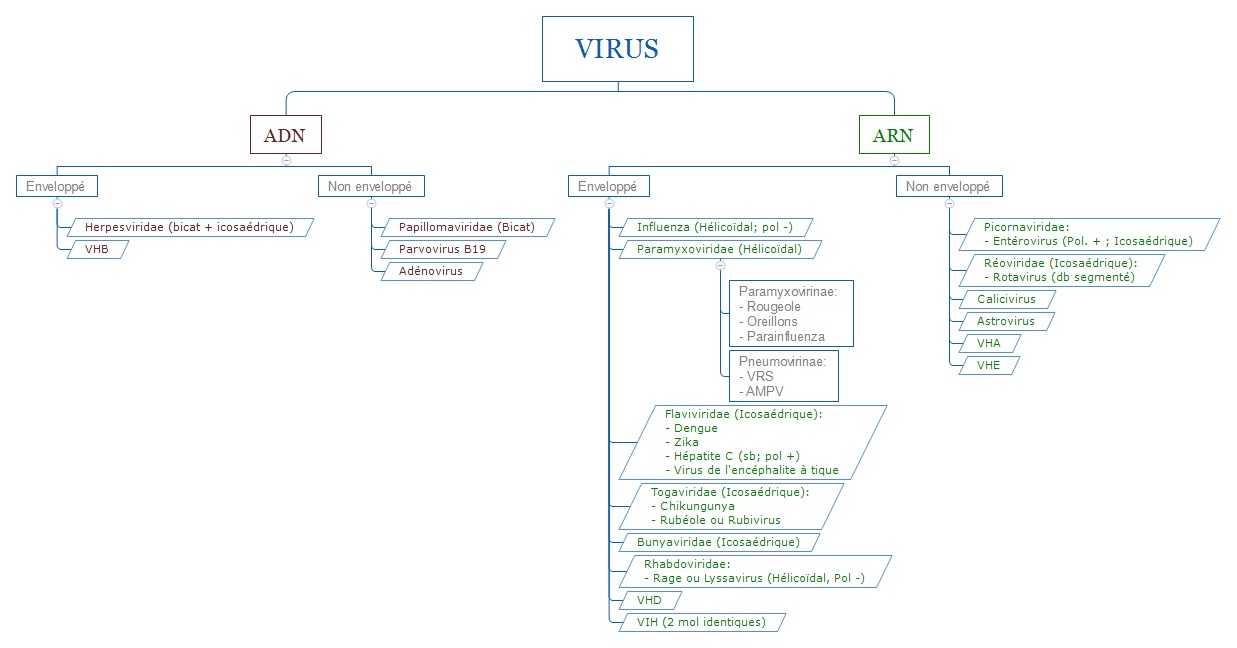
b: Principaux virus pathogènes pour l'homme:
D/La multiplication des virus animaux :
On les appelle "virus animaux" car ils se multiplient à l'intérieur des cellules vivantes.
L'interaction la plus simple entre un virus et une cellule et l'interaction dite lytique: en se multipliant, le virus entraîne la lyse ou la mort de la cellule infectée qui libère ainsi les particules virales néoformées. Mais, il existe des interactions complexes telles que la persistance et la transformation.
- la persistance: la cellule infectée continue de vivre en hébergeant un virus dont les niveaux d'expression sont variables et qui vont de la latence à l'infection chronique productive.
- la transformation : elle résulte souvent de l'intégration de la totalité ou d'une partie du génome viral dans le génome cellulaire. la cellule acquiert de nouvelles caractéristiques morphologiques et biologiques. Sa vitesse de croissance va notamment augmenter et cette cellule transformée est à la base du processus d'oncogenèse virale.
Le comportement d'un virus n'est pas univoque. Il dépend du type cellulaire rencontré et de la réponse immunitaire de l'organisme. Par exemple, le virus herpétique peut connaître des phases alternées de lyse et de latence.
Nota béné: Il est important de garder à l'esprit que nous sommes le fruit du chaos et les descendants d'épidémies avec un génome où 2% de gènes sont surclassés par 98% de séquences parasites. Notre patrimoine génétique est issus de rencontre avec des virus, des bactéries et autres organismes qui ont intégrés pour certains d'entre eux dans notre génome des séquences génétiques plus ou moins exprimées.
La multiplication virale lytique :
-schématiquement, les phases de la multiplication virale sont les suivantes :
-l'absorption du virus sur la membrane cellulaire (généralement au niveau des récepteurs spécifiques). Si ces récepteurs cellulaires sont absents, le virus ne pourra pas se multiplier.
- la pénétration et la décapsidation qui à l'exception des poxviridae est toujours le fait d'enzymes cellulaires.
-la synthèse de protéine virale et la réplication du du génome viral.
-l'assemblage des nucléocapsides dans le cytoplasme ou le noyau de la cellule infectée.
-la libération virale.
Étude des réplications lytiques des virus ARN et des virus ADN :
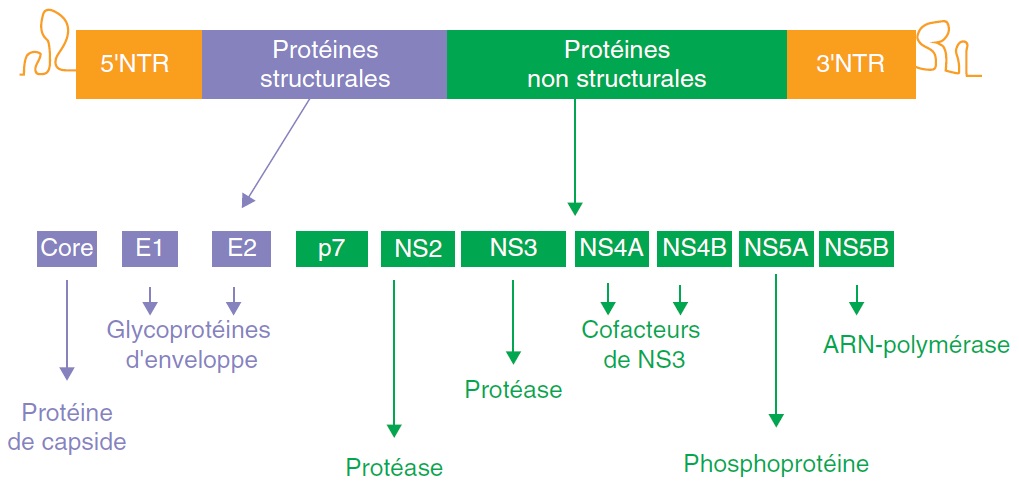
V
irus à ARN+ de l’hépatite C (VHC). Identifié en 1989, Famille des Flavivirida Genre HépacivirusSource:https://aemip.fr/wp-content/uploads/2022/10/image-58.png
a/ Les virus à ARN:
On distingue les virus ARN positifs (+) et à ARN négatifs ( -).
a/ ARN +
L'ARN génomique (+) va servir directement d'ARN messager. C'est le cas par exemple pour le virus de la poliomyélite.
Le virus se fixe sur un récepteur spécifique de la cellule puis pénètre dans une vacuole de pinocytose et subit une décapsidation non spécifique assurée par les enzymes cellulaires(1).
L'ARN viral libéré sert directement de matrice pour les ribosomes (2)
Un polypeptide unique Noo est synthétisé et il sera ensuite clivé en N1, Nx et N2. N1 est à son tour clivé en VP0, VP1 et VP3 qui sont les protéines constitutives de la procapside. Nx et N2 vont constituer une ARN polymérase ARN dépendante appelée ici réplicase.
La réplicase va synthétiser un brin complémentaire de l'ARN viral (+). Ce brin est dit négatif (-). L'ARN bicaténaire qui apparaît est appelé complexe de réplication (3).
La réplicase va ensuite utiliser un brin (-) néo synthétisé pour fabriquer de nombreux brins (+) dans une structure appelée intermédiaire de réplication (4).
Les brins (+) néo synthétisés vont servir à la synthèse protéique ou être incorporée d'abord dans une procapside constituée de protéines VP0, VP1 et VP3, puis ensuite dans la capside définitive dont la fermeture est assurée par le clivage de VP0 en VP2 et VP4 (5).
Les virions complets s'accumulent alors dans le cytoplasme. La cellule peut se lyser approximativement au bout de 7h et libérer quelques milliers de virions.
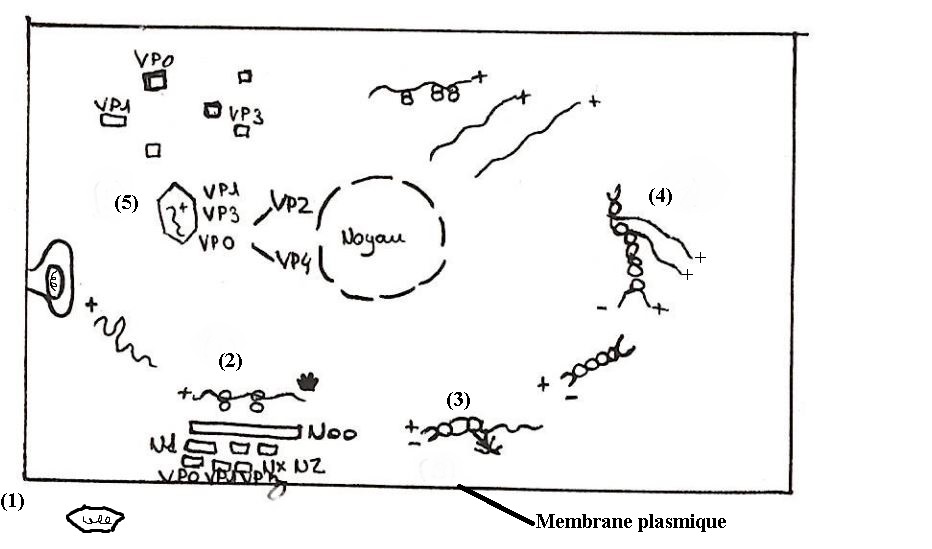
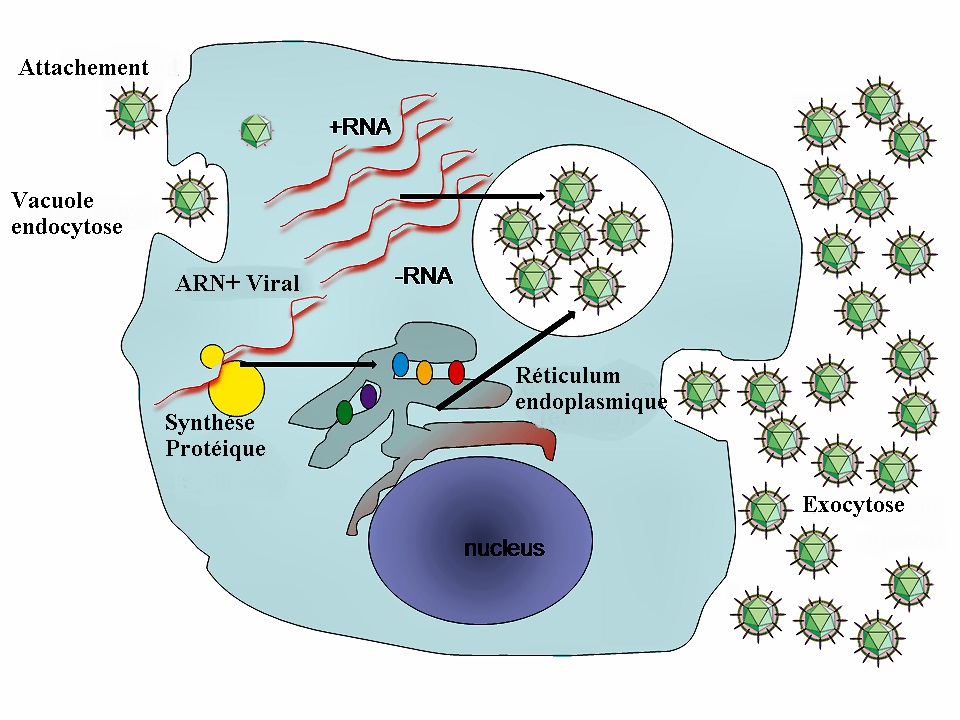
Source: https://aemip.fr/wp-content/uploads/2022/10/image-58.png
b/L'ARN -
ARN (-)
Le virus que je vais choisir est celui du paramyxoviridae, genre paramyxovirus et plus précisément le virus para influenza 1 qui peut donner des infections virales respiratoires. Les cellules cibles de ce virus sont les cellules épithéliales ciliées de l’arbre respiratoire. Le virus s’y multiplie et diffuse de proche en proche. Il peut atteindre à partir du rhinopharynx, les voies respiratoires inférieures : le larynx, les bronchioles.. L’élimination du virus est rapide chez le sujet immunocompétent.
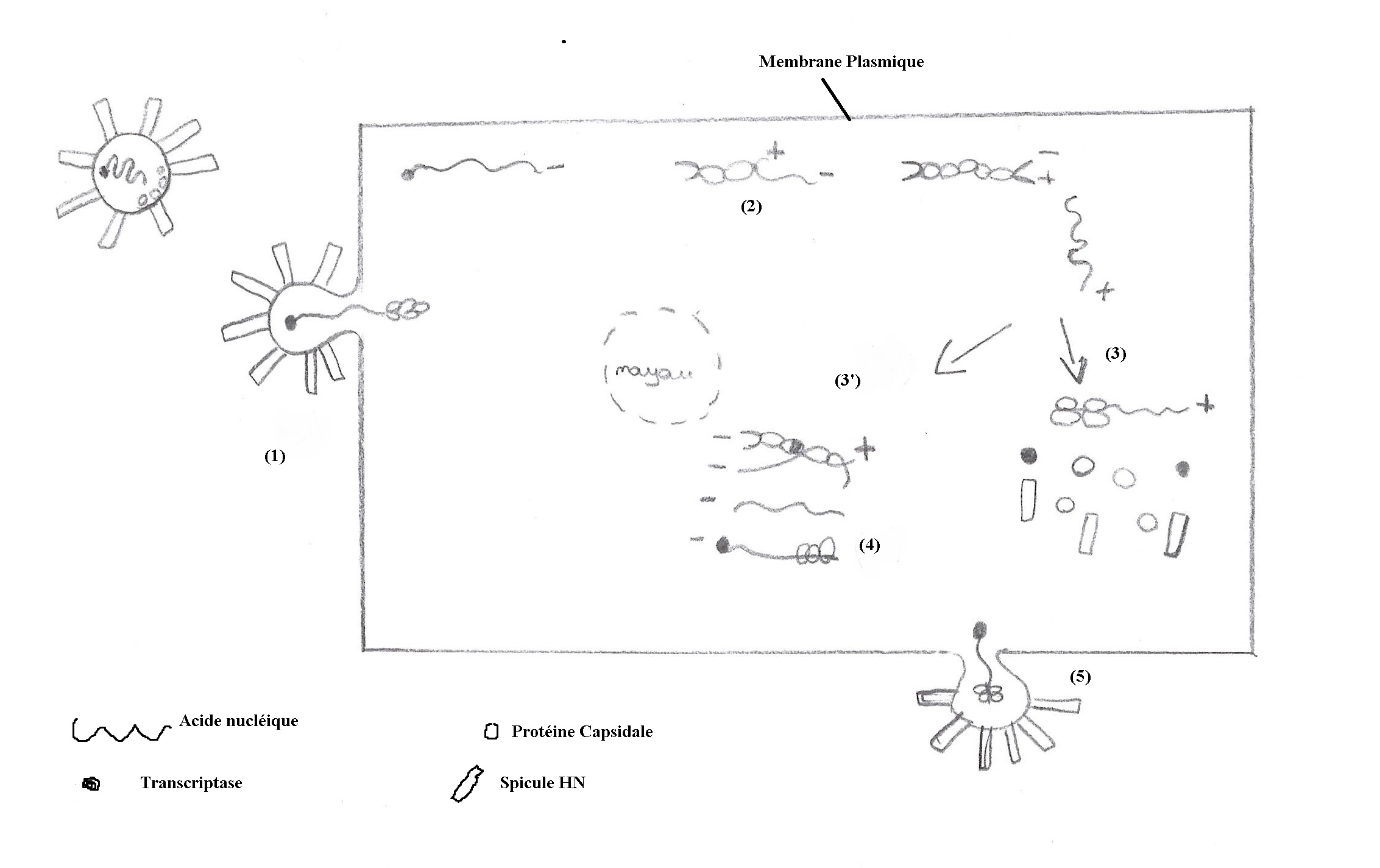
L’ARN viral ne pouvant pas servir directement d'ARN messager est dit négatif (-) et obligatoirement associé dans la particule virale à une enzyme ARN polymérase ARN dépendante, appelée transcriptase. L’ensemble ARN (-) transcriptase est dans une capside hélicoïdale pelotonnée à l'intérieur d'une enveloppe hérissée de spicules présentant une activité hémagglutinante et neuraminidasique (HN).
Le virus se fixe par l'intermédiaire d'un de ces spicules sur un récepteur spécifique de la membrane cytoplasmique cellulaire (1).
L'enveloppe virale fusionne avec la membrane plasmique, la nucléocapside pénètre dans le cytoplasme puis est dégradée libérant ainsi l'ARN (-) associé à sa transcriptase. L'enzyme synthétise alors un ARN (+) à partir de l'ARN (-) virale (2).
Cet ARN (+) sert d'ARN messager et est traduit en protéine virale (3).
Il sert également de matrice pour la synthèse d'ARN (-) (3’) qui sera encapsidé (4).
Les nucléocapsides s'accumulent dans le cytoplasme cellulaire. Le stade final est celui du bourgeonnement (5) où des nucléocapsides viraux traversent la membrane plasmique hérissée de spicules. Le virus enveloppé est ensuite libéré. La cellule va mourir sans effraction. Le cycle de réplication est d'environ 18h.
c/Les virus à ADN
1/ les adénovirus
L'adénovirus possède un ADN bicaténaire linéaire dans une capside icosaédrique dont les pentons portent une fibre hémagglutinante.
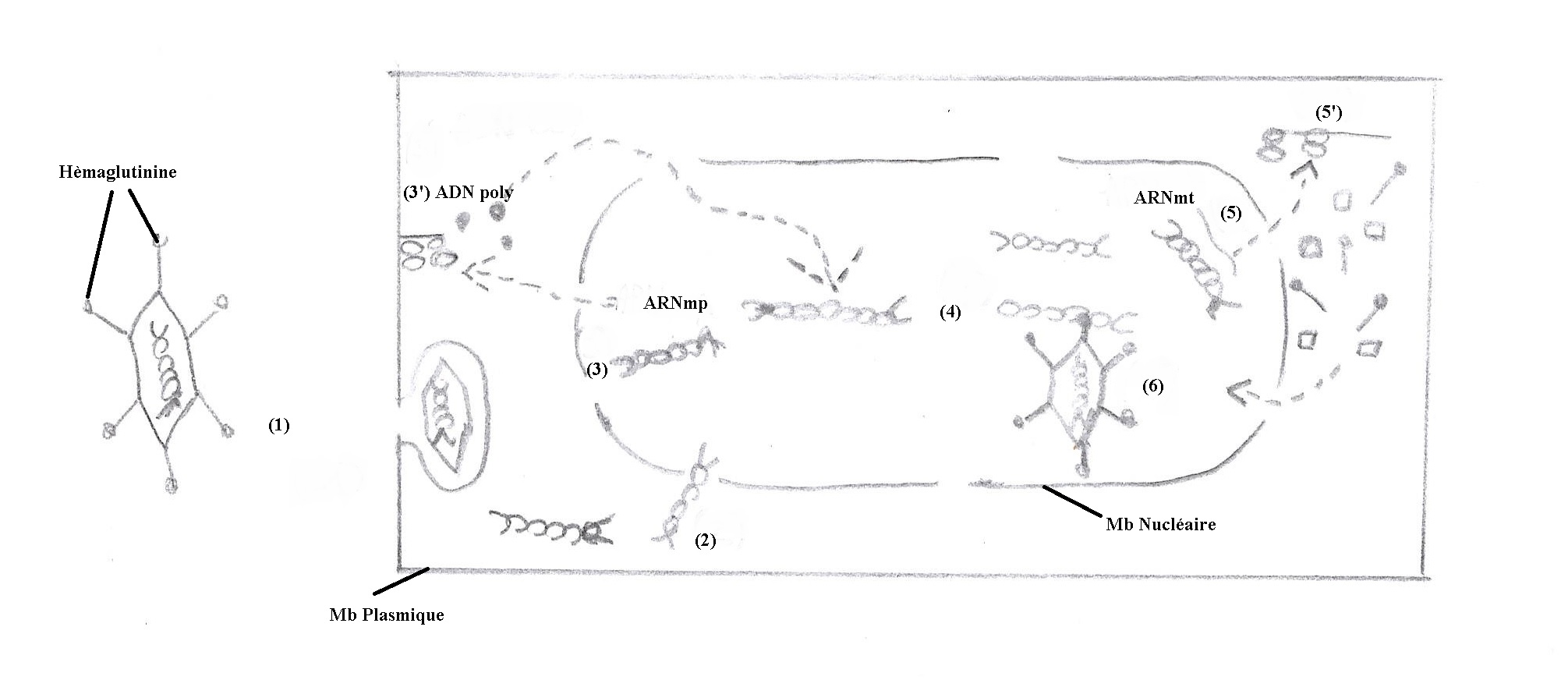
Le virus se fixe sur la cellule par l’intermédiaire de son hémagglutinine puis pénètre dans une vacuole de pinocytose (1).
Après la décapsidation, l'ADN viral migre dans le noyau cellulaire (2), il y a alors transcription précoce grâce à un ARN polymérase ADN dépendante et apparition d'ARN messagers précoces qui ne correspondent qu'à une petite partie du génome viral (3).
Ces ARNmp (ARN messagers précoces) passent dans le cytoplasme où ils sont traduits en protéines précoces (notamment une ADN polymérase) (3’). L'ADN polymérase va gagner le noyau où elle duplique l'acide nucléique virale (4). Sur les acides nucléiques viraux néoformés, on assiste à une transcription tardive (5) qui intéresse la totalité du génome viral, les ARN messagers tardifs correspondant sont traduits en protéines de structure (5’) qui repasse dans le noyau où s'effectue l'assemblage de la nucléocapside (6).
Généralement les nucléocapsides s'accumulent dans le noyau au bout d'environ 32 à 34 heures. La cellule va se lyser en libérant les particules virales néoformées.
Ce cycle de réplication est le plus courant pour les adénovirus mais il y a des particularités pour un certain nombre d'autres virus.
2/ Particularité des herpesviridae et des poxviridae.
Le schéma de la réplication est le même que pour l'adénovirus. Il existe pendant quelques particularités :
a/ Herpesviridae:
La nucléocapside est assemblée dans le noyau mais elle s'enveloppe en traversant la membrane nucléaire. Le virus complet va cheminer dans une citerne du réticulum endoplasmique jusqu'à la périphérie cellulaire.
b/ Poxviridae:
La décapsidation est spécifique c'est-à-dire qu'elle est codée par le virus.
Le cycle de multiplication et l'assemblage de la nucléocapside sont strictement intracytoplasmique.
F/Conséquences au niveau de la cellule et applications :
L'infection virale retentit sur les synthèses des macromolécules cellulaires qui sont en général rapidement bloquées ou fortement diminuées. La lyse cellulaire va généralement s'accompagner d'un effet cytopathique (ECP), c'est-à-dire une anomalie cellulaire appréciable en microscopie photonique et qui est caractéristique du virus (ou de la famille du virus) infectant.
La connaissance de cette ECP est importante pour le diagnostic virologique en pratique courante.
On peut au laboratoire effectuer le titrage d'une suspension virale. On effectuera une culture cellulaire avec des dilutions croissantes de la suspension virale. La dernière dilution pour laquelle se manifeste un ECP permet de calculer le nombre de particules virales dans un volume déterminé. La multiplication virale étant intimement liée à la vie cellulaire, on comprend toute la difficulté qui existe à développer une chimiothérapie antivirale qu'il ne soit pas en même temps anti-cellulaire.
E/ Évolution génétique des virus
Les recherches ont permis de mettre en évidence la capacité des virus à muter et cela grâce à des marqueurs faciles à mettre en évidence.
Ces virus mutants ont été utilisés comme des sondes spécifiques pour étudier les phénomènes génétiques et biochimiques qui ont lieu au cours de l'infection virale. Les virus sont tout en bas de l'échelle de la complexité des agents biologiques. Leur fonctionnement est très complexe et la diversité du groupe est très large. Les virus sont des structures biologiques relativement simples puisqu'ils sont essentiellement constitués de quelques gènes libres, parfois associés à un minimum de matériel annexe (capside, enveloppe, enzyme, protéine de surface ,...).
1/Méthode d'étude des génomes viraux:
Au début du développement de la virologie, les méthodes d'études de la structure des génomes viraux était relativement compliquée et faisait intervenir l'analyse antigénique à l'aide d'anticorps monoclonaux pour faire la cartographie des fragments de gènes après digestion enzymatique partielle ou l'hybridation moléculaire ARN-ADN ou ADN-ADN.
Cela dit, les résultats étaient intéressants confirmant les données obtenues par l'analyse génétique.
Grâce au progrès rapide des méthodes de biologie moléculaire, aujourd’hui, on peut rapidement déterminer directement la séquence d'un gène même sur une petite quantité de matériel : clonage et amplification génique, PCR, séquençage automatique,... et donc il est possible de comparer les séquences de gènes voire même le génome complet de deux virus voisins ou de deux mutants du même virus. Les modifications de séquence peuvent être comparées au changement des propriétés biologiques et le sens de l'évolution des virus peut ainsi être suivi.
2/Stratégies d'expression des génomes:
La diversité de structure des virus ADN ou ARN, polarité des ARN, présence ou absence d'enveloppe, forme de symétrie de la capsule, a pour conséquence une variété considérable de leur mode de multiplication et en particulier de leur stratégie de réplication. J'entends par là, la manière dont s'enchaînent tous les événements du cycle de réplication des acides nucléiques qui conduisent le virus infectant à faire produire une quantité importante de nouveaux virus ou à modifier les activités cellulaires. Beaucoup d'étapes restent communes à tous les virus, au moins dans leur principe : fixation sur la cellule cible, pénétration à l'intracellulaire, perte de l'enveloppe et ou de la capsule (décapsidation), réplication des acides nucléiques, synthèse et protéines, assemblage, maturation, sortie hors de la cellule par lyse ou par bourgeonnement. La structure et le fonctionnement du matériel génétique du virus sont au centre de ce de ces processus.
3/ Les virus défectifs interférents :
Il existe des virus défectifs incomplets et connus depuis très longtemps.Le passage successif sur l'embryon de poulet d'une souche de virus grippal en utilisant des préparations de virus non dilué quel que soit leur richesse en virus, provoque des phénomènes d'accumulation de virus défectif, incapable de se multiplier. Une quantité importante de virus est produite mais pour la grande majorité d'entre eux, ils sont sous forme non infectieuses. Les virions produits sont décelables, il sédimentent lors d'une centrifugation, leur aspect morphologique est équivalent à celui d'un virus normal, les protéines ne représentent pas d'anomalie, mais on y trouve pas les ARN attendus:: ces virus sont incomplets et non infectieux. Lorsque cours des passages, c'est la proportion de ce type de virus augmente, des phénomènes d'interférence se produisent avec la réplication du virus normal et le titre de celui qui baisse. On observe alors des fluctuations qui font alterner des passages hautement productifs et d'autres où le virus défectif domine. L'origine de ce phénomène est une délétion d'une partie de l'ARN. Le virus qui porte ce défaut est ensuite amplifié au cours des passages par une réplication concomitante des particules normales et défectives, les secondes étant complémentés par les premières. La probabilité pour qu'une cellule soit infectée simultanément par un virus de chaque catégorie augmente évidemment avec la multiplicité d'infection.
F : Les mutations
1/Mutation spontanée et hétérogénéité génétique :
Les mutations spontanées portent sur un certain nombre de caractères ou marqueurs qui permettent de les tester mais bien d'autres surviennent sans doute et échappent à notre détection. Ses caractères sont très variés ils peuvent concerner le taux de réplication, l'expression des plages de lyse cellulaire, le pouvoir pathogène, le spectre de l’hôte, la résistance à certains agents chimiques ou physiques. Pour les virus qui ont un taux élevé de mutations spontanées, on peut constater une grande hétérogénéité, non seulement d'un virus à l'autre ou d'une souche à l'autre, mais même au sein d'une même souche, c'est-à-dire d'une population naturelle. Les observations de ce genre ont été faites pour certains virus à ARN.
2/Mutation induite :
Les mutations induites par des agents mutagènes portent sur les mêmes caractères mais apparaissent avec une plus grande fréquence et peuvent être sélectionnées dès le premier site de réplication par des facteurs appropriés. Les agents mutagènes utilisables pour créer de nouveaux caractères chez les virus sont très nombreux et appartiennent à plusieurs catégories.
On peut utiliser des mutagènes in vitro qui modifient l'acide nucléique virale en dehors des cycles de réplication par contact direct avec des virions. Exemple : l'acide nitreux transforme l'adénine en hypoxanthine ou transforme la cytosine en uracile modifiant ainsi le code génétique du virion. Des agents alkylants (utilisés en cancérologie pour empêcher la cellule de se diviser) comme le N méthyl N’- nitro N- nitroso- guadisine ou encore la N méthyl-N nitrosourée provoque une modification de structure en méthylant les guanines (très cancérigène).
Il existe également des agents mutagènes qui agissent in vivo durant la réplication des acides nucléiques comme des analogues de bases incorporés dans la structure des molécules en cours de synthèse et donnant des produits anormaux. En effet, ces derniers provoquent des remaniements moléculaires. Par exemple : le 5 fluorouracile s'incorpore très efficacement à la place de l'uracile jusqu'à 50 % de substitution inversant l'adénine avec la guanine mais aussi l’uracile avec la cytosine en modifiant ainsi le code génétique du virus.
Des agents intercalants (comme les colorants acridines1 comme la flavine ou ses dérivés) peuvent s'insérer dans l’hélice d’ADN en provoquant des distorsions, des insertions ou des délétions modifiant ainsi le code génétique.
Enfin les rayons ultraviolets sont capables également de provoquer des mutations chez les virus à ADN comme les virus ARN plus sensibles.
Il est à noter que les mutations induites peuvent être corrigées par des réversions, spontanées induites dont il est possible de mesurer leur fréquence.
3/Différents types de mutants :
-Il existe des mutants thermosensibles (ts), ils sont majoritaires, ils sont dénommés létaux thermosensibles et apparaissent qu'à des températures relativement élevées. Les virus ne peuvent pas exprimer tous leurs gènes si les températures sont trop élevées. Seules certains gènes plus thermorésistants arrivent à être lus ce qui fait que le virus ne s'exprime qu'en partie. On utilise beaucoup les virus ts pour les expériences d'analyses mais il faut sélectionner les plus stables.
-Il y a aussi des virus de plages où la taille et l'apparence des plages de lyse sur des tissus cellulaires in vitro qui sont caractéristiques de chaque virus (nature des cellules sensibles, conditions de culture, besoins de composants nutritifs spécifiques,). Ces spécificités permettent de sélectionner certains virus grâce à ces plages de spécificité et d'avoir des souches très pures. Grâce à cela, on peut, entre autres étudier la stabilité des populations virales.
Cette méthode des plages virales est une technique de référence pour compter les particules virales infectieuses dans un échantillon. Cette méthode repose sur la capacité des virus à former des zones claires appelées plages de lyse sur une culture cellulaire.
Le principe est très
simple. On peut faire une analogie avec une pelouse de cellules cultivées en
laboratoire. Lorsqu'un virus infecte une cellule, il se multiplie et détruit les
cellules environnantes, créant une zone circulaire transparente. Chaque plage
correspond théoriquement à un seul virus initial.
Cette technique permet de mesurer le titre viral, c'est-à-dire le nombre
d'unités formant une plaque (UFP) par millilitre d'échantillon. L'intelligence
artificielle permet d'automatiser le comptage des plages, réduisant les erreurs
humaines de 40%. Cette méthode automatisée (IA) peut s'appliquer à de nombreux
types de virus : bactériophages2, virus animaux, virus
végétaux et peut analyser jusqu'à 500 échantillons par jour.
Acridines1 : L'orange d'acridine est une coloration fluorescente précieuse en microbiologie en raison de sa capacité à se lier aux acides nucléiques et à produire une fluorescence différentielle.
Bactériophages2 : Définition, morphologie et rôles :
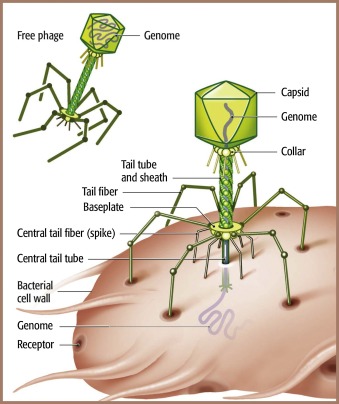
Source : https://www.sciencedirect.com/topics/medicine-and-dentistry/bacteriophage
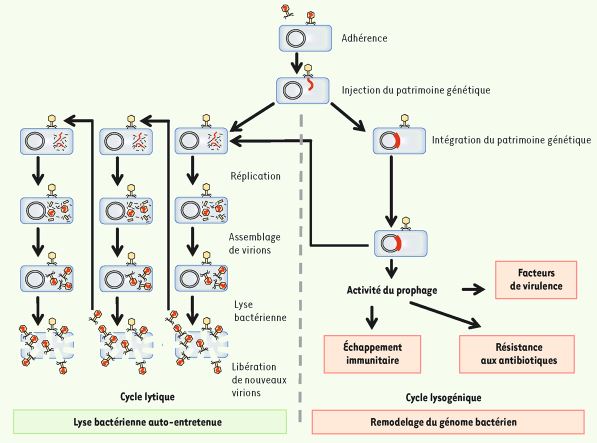
Les bactériophages (ou phages) sont des virus naturels qui infectent les bactéries. Ils sont très répandus dans l’environnement tellurique et aqueux (eau salée, douce et égouts). Les phages vivent avec les bactéries qu'ils infectent (depuis quelques milliards d'années). Très souvent, chaque phage est spécifique d'une seule espèce bactérienne, voire même d'une population clonale. Il en existe une grande diversité. Virale. La grande majorité des espèces appartiennent à l'ordre des Caudovirales, et en particulier aux familles Myoviridae (phages ayant une queue contractile), Podoviridae (queue courte et non contractile) et Siphoviridae (queue longue filamenteuse et non contractile), avec des protéines structurales conservées qui forment ces différentes particules virales. Les phages jouent un rôle majeur dans l'équilibre écologique du monde bactérien. En fonction de leur activité sur leur bactérie hôte, deux types de phages existent. Les phages tempérés, qui accomplissent un cycle lytique et lysogénique. Les phages virulents, qui n'accomplissent qu'un cycle lytique. Au cours du cycle lysogénique, le génome des phages s'intègre dans le génome bactérien sous la forme d'un « prophage ». Souvent ils contribuent à enrichir le patrimoine génétique de la bactérie, en y intégrant des gènes codant différents facteurs. Des gènes de virulence, de toxines, des facteurs facilitant l'échappement à l'immunité, ou encore des gènes de résistance aux antibiotiques. Parfois, le prophage peut s'exciser et infecter une autre bactérie environnante de la même espèce en reprenant un cycle lytique. Lors d'un cycle lytique, les phages détournent la machinerie cellulaire bactérienne pour produire par centaines de nouveaux virions. Les bactériophages provoquent ensuite la lyse de la bactérie hôte par la production de protéines virales comme « endolysine » qui dégrade le peptidoglycane (paroi bactérienne) ou la holine qui forme des pores dans la membrane plasmique de la bactérie.
Cette lyse va libérer de nouveaux virions qui vont à leur tour infecter les bactéries environnantes.
Cela peut conduire à la disparition complète de la communauté bactérienne. La phagothérapie (thérapie virale par phages) consiste donc à isoler des phages naturels virulents (dans l'environnement humain), les cultiver et les purifier pour traiter diverses infections bactériennes.
Source : https://www.sciencedirect.com/topics/medicine-and-dentistry/bacteriophage
4/ Mélanges phénotypiques :
Les glycoprotéines de surface d'un virus particulier peuvent s'incorporer dans l'enveloppe d'un virus différents au moment de l'assemblage et donner alors un pseudotype ou un phénotype. Il ne s'agit pas d'un phénomène génétique puisque le génome viral de l'hôte reste identique et ne donnera que ce pourquoi il est "programmé". Ce dernier aura une spécificité momentanément de par ses glycoprotéines et les réactions immunitaires ne seront pas forcément les mêmes.
5/Variation antigénique :
Le virus de la grippe est très largement étudié pour son exceptionnel variabilité depuis plus de plus de 45 ans. Connaître à un instant "t" le gène qui commande son hémagglutinine (glycoprotéine de structure) qui est particulièrement impliqué dans la réponse immunitaire permet de mettre au point des stratégies thérapeutiques. La mise au point vaccin contre la grippe n'est pas la panacée car le virus mute trop rapidement pour qu'il soit vraiment efficace. De plus, l'émergence de souches mutantes est facilitée par le niveau d'immunité de la population humaine exposée au virus. En effet, le système immunitaire ne reconnaît pas le nouvel antigène et permet au virus de se propager et provoquer des épidémies. Pour le vaccin soit efficace il faut donc cibler un antigène générique de la souche ce qui assez compliqué à fabriquer.
Il faut garder à l'esprit aussi que d'autres mécanismes interviennent dans la variabilité des virus. Si on étudie les virus grippaux avec un isolement à plusieurs reprises chez une personne, on constate que les infections doubles (par exemple : H1N1& H3N2), sont extrêmement répandues. Il y a très souvent un réassortiment entre virus et donc beaucoup de variants dans une même population. Le virus de la grippe est très largement étudié pour son exceptionnel variabilité depuis plus de plus de 45 ans. Connaître à un instant « t » le gène qui commande son hémagglutinine (glycoprotéine de structure) qui est particulièrement impliqué dans la réponse immunitaire permet de mettre au point des stratégies thérapeutiques ; La mise au point vaccin contre la grippe n'est pas la panacée car le virus mute trop rapidement pour qu'il soit vraiment efficace. De plus, l'émergence de souches mutantes est facilitée par le niveau d'immunité de la population humaine exposée au virus. En effet, le système immunitaire ne reconnaît pas le nouvel antigène et permet au virus de se propager et provoquer des épidémies. Pour le vaccin soit efficace il faut donc cibler un antigène générique de la souche ce qui assez compliqué à fabriquer.
Il faut garder à l'esprit aussi que d'autres mécanismes interviennent dans la variabilité des virus. Si on étudie les virus grippaux avec un isolement à plusieurs reprises chez une personne, on constate que les infections doubles (par exemple : H1N1& H3N2), sont extrêmement répandues. Il y a très souvent un réassortiment entre virus et donc beaucoup de variants dans une même population.
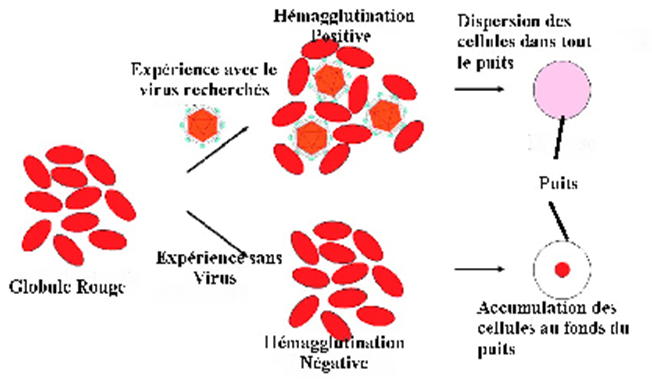
Pour le virus de la grippe, on peut sélectionner les mutants avec des Anticorps spécifiques de l’Antigène initial, car on dispose d'Anticorps monoclonaux avec une très grande spécificité. On peut par conséquent utiliser cette pression sélective pour obtenir des mutants choisis à l'avance pour être spécifique d'un épitope1 donné. On peut alors en déterminant la séquence des virus parents et mutés, identifier avec précision les sites de mutation correspondant au changement antigénique observé. Le rapport de ces indications sur le modèle tridimensionnel de l'hémagglutinine du virus a permis de définir des domaines hypervariables de cette structures et de les localiser sur le modèle moléculaire de cette protéine importante. Cette méthodologie s'applique à la très grande majorité des virus.
Les épitopes1 sont des régions spécifiques des antigènes qui sont reconnues par le système immunitaire. Quand le système immunitaire reconnaît ces épitopes comme étant étrangers à l'organisme, il réagit.
6/ Taux de mutations : Les mutations sont à cause principale de la variation du génome des virus. Le taux de mutation est la probabilité qu’un virus mute au cours d’une seule réplication où un nucléotide soit modifié par substitution, délétion, insertion ou encore recombinaison. Certains virus sont des champions dans ce domaine. Les virus à ADN ont des taux beaucoup plus faibles (de 10-8 à 10-11 par nucléotide incorporé) alors que les virus à ARN les taux sont beaucoup plus élevés (de 10-3 à 10-4 par nucléotide incorporé). En fonction des milieux de culture ce taux peut être favorisé ou inversement. Si les variations sont si courantes pour les virus à ARN, c’est que les erreurs de réplication sont très courantes. Pour cette raison la taille du génome ne peut pas trop s’accroitre et est va de 3,5 kilobases (rétrovirus) à 27 kilobases (certains réovirus). Pour les virus segmentés, la contrainte est moins sévère car chaque segment peut attendre cet ordre de grandeur. Des observations ont mis en évidence que le taux de mutations diminuait lorsque la taille du génome augmentait.
G : Interactions génétiques :
1/Recombinaison génétiques :
La recombinaison génétique est un phénomène bien établi. On a pu au laboratoire produire des recombinants intra ou interspécifique de poliovirus ou de virus de la fièvre, après infection mixte et on a trouvé des recombinants naturels du 1er de ces agents dans l'intestin humain au cours de l'affection naturelle. Le même phénomène est connu aussi chez des coronavirus. La complémentation est plus rare chez les virus à génome segmenté de polarité négative. On a observé une réactivation par infection multiple de certains virus. En effet, des virus inactivés par les rayons ultraviolets peuvent être réactivés par infection multiple. Lorsque la multiplicité d'infection augmente, le nombre de plages augmente plus vite que ne le voudrait la proportionnalité : le virus partiellement inactivé se complémente automatiquement lui-même.
2/ réassortiment :
Le réassortiment consiste en réarrangement des segments de nucléocapside au moment du bourgeonnement à la surface de la cellule, au moment où le virus assemble ses segments pour la formation de virion complète. Si une même cellule a été infectée simultanément par deux virus (ou plus) et s'il y a des virus qui ont multiplié leur ARN, l'assemblage final des nucléocapsides peut se produire en incluant au hasard des segments de chacun des deux virus (ou plus encore). Les infections mixtes ne sont pas rares et sont très simples à reproduire expérimentalement. On a pu mettre en évidence à plusieurs reprises dans ces systèmes, des infections doubles résultant en une recombinaison de deux ou voir même plus de virus encore.
On connaît un exemple historique pour lequel la recombinaison naturelle a pu se faire. Il s'agit de la naissance du virus H3N2, qui résulte du réassortiment du virus H2N2, virulent pour l'homme qui avait circulé entre 1958 et 1968, avec un virus aviaire connu depuis 1963 (A/Duck/Ukraine H3N8). Un échange d'hémagglutinine entre les deux virus a produit la combinaison H3N2, toujours virulente pour l'homme et doué d'une hémagglutinine nouvelle et par conséquent libre de toute barrière immune. Ce virus a causé une pandémie meurtrière dès son apparition en 1968 (grippe de Hong Kong).
3/Interaction avec les cellules et transformation :
La transformation maligne (cancer) est le processus par lequel une cellule normale de l'organisme devient une cellule cancéreuse. Elle peut être induite par différents événements (par exemple, par l'exposition aux carcinogènes chimiques ou l'irradiation ionisante, …), mais aussi par l'infection virale. La transformation comprend souvent une perte de contrôle de la croissance, la croissance indépendante de l'ancrage de la cellule, la capacité d'envahir la matrice extracellulaire, la dédifférenciation et l'immortalisation.
La perturbation des contraintes normales sur la prolifération cellulaire qui caractérise la transformation maligne ne peut se produire que d'un nombre de façons strictement limité, et il peut y avoir aussi peu que quarante gènes cellulaires chez lesquels une mutation ou une autre perturbation de leur expression conduit à une croissance cellulaire non contrôlée.
Il y a deux classes de ces gènes dont l'expression altérée peut entraîner une transformation maligne :
-Les gènes qui stimulent la croissance et qui provoquent le cancer lorsqu'ils sont hyperactifs. Des mutations dans ces gènes seront dominantes. Ces gènes sont appelés des oncogènes.
-Les gènes qui inhibent la croissance des cellules, et qui provoquent le cancer lorsqu'ils sont inactivés. Des mutations dans ces gènes seront récessives. Ce sont les anti-oncogènes ou des gènes suppresseurs de tumeurs. L'étude des virus qui provoquent des cancers chez les rongeurs et chez les oiseaux a été extrêmement importante dans l'identification des oncogènes et des anti-oncogènes.
Chez l’homme des virus au pouvoir oncogène sont capables d’induire la formation de tumeurs caractérisées par la transformation cellulaire. Les cellules infectées sont immortalisées et elles présentent des caractéristiques particulières. Elles sont capables de transmettre et de produire des cellules malignes si elles sont inoculées à des animaux immunodéprimés. Elles ont un potentiel de culture supérieur à celui de cellules normales. Elles se divisent indéfiniment, perdent tout contact d’inhibition, ont une haute efficacité de clonage et ont des besoins nutritifs réduits. Elles présentent des anomalies morphologiques et chromosomiques.
L’Oncogène viral est exprimé par le virus où une ou plusieurs protéines perturbant la division cellulaire est synthétisée.
La mutagénèse insertionnelle est l’insertion du génome viral dans le génome cellulaire qui va entraîner une prolifération incontrôlée des cellules.
Les cycles de nécrose/régénération sont des mécanismes indirects de l’oncogenèse viro-induite. Ce mécanisme est évoqué pour les hépatocarcinomes liés aux virus des hépatites B et C.
Quelques exemples de cancers associés aux virus peuvent être cités qu’il s’agisse de virus à ADN comme l’EBV (lymphome de Burkitt, carcinome du naso-pharynx), l’HBV (carcinome hépatocellulaire) ou du virus à ARN et l’HTLV1 (leucémie T, lymphomes) HCV (carcinome hépatocellulaire).
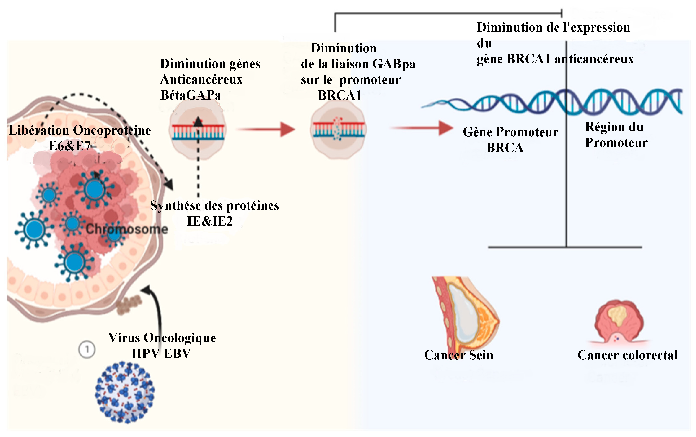
Source : https://www.mdpi.com/1718-7729/30/2/150
L’intégration de séquence d’ADN virale dans une cellule semble se faire au hasard. Pour mettre en évidence ce phénomène de l’intégration on utilise la recherche de la présence de portion de gènes viraux dans l’ADN cellulaire par une extraction de celui-ci suivie d’un traitement par les protéases et ribonucléases. On recherche après cela les séquences virales dans l’ADN extrait des cellules par hybridation moléculaire avec une sonde constituée d’ADN virale marqué. Une hybridation positive est mesurée par la formation de molécules hybrides repérables grâce au marquage.
4/ La Virulence :
Les facteurs de virulence sont les fonctions qui permettent à des virus de causer une maladie. Ils répondent à la version moléculaire des postulats de Koch. Se sont des fonctions virales qui permettent la multiplication du virus au site d‘entrée. Pour faciliter la compréhension, je vais aborder la stratégie que mette en place certains virus. La neurovirulence1 est une propriété essentielle de la pathogénie des infections à alphaherpèsvirus (sous-famille des virus Herpesviridae). La relation qui s‘est établie entre ces virus et leurs hôtes immunocompétents est responsable de l‘acquisition par les premiers de stratégies d‘échappement aux constituants de la réponse immune des seconds. Dans la description des différentes tactiques d‘échappement au système immunitaire, un accent particulier est mis sur le mécanisme de la « latence‐réactivation » qui permet aux alphaherpèsvirus de persister à vie chez leurs hôtes tout en se disséminant de manière périodique. Malgré la diversité des agents infectieux envisagés et des pathologies qu‘ils entraînent, l‘étude des bases moléculaires de la virulence des alphaherpèsvirus constitue la clé de voûte de la compréhension de la pathogénie de ces infections.
En effet, une meilleure compréhension des fonctions virales qui permettent à un virus de causer une maladie a ouvert la voie à la mise au point d'agents chimio thérapeutiques antiviraux. De plus, la sélection de souches vaccinales sûres repose, sur une connaissance des facteurs de virulence. Fondamentalement, la complexité de la virulence des alphaherpèsvirus montre que ces derniers ont subi un processus évolutif responsable de l'acquisition de propriétés essentielles au maintien de la relation hôte-virus. La latence doit être considérée comme une garantie de pérennité d'une infection virale dans une population aussi bien humaine qu'animale. De plus, grâce à la maîtrise de facteurs de virulences particuliers, les herpèsvirus constituent des outils qui permettent de les utiliser dans les thérapies géniques du cancer.
Lors d’infection multiples des échanges de gènes peuvent avoir lieu entre différents les virus comme on l’a vu.
Des virus non virulents peuvent le devenir et réciproquement donnant alors des variants.
Conclusion ! En microbiologie les germes ne sont pas statiques mais en perpétuelle évolution.
Ils échangent en permanence avec leur environnement et parfois peuvent sauter la barrière des espèces. Ces vingt dernières années on a pris conscience le fait que les virus franchissent parfois la barrière des espèces, cela conduit à l'émergence de maladies virales dans de nouvelles espèces hôtes.
La neurovirulence1 : Certains agents infectieux touchent plus spécifiquement les nerfs périphériques comme par exemple le zona, très fréquent, ou le bacille de Hansen, agent de la lèpre. De même le virus de la varicelle pour le cervelet, ou le virus herpès simplex pour l'encéphale.
1/ Technique d'analyse de la cellule
5/ Appareil de Golgi ou Dictyosome
13/ Complément sur la méthodologie de recherche en biologie cellulaire